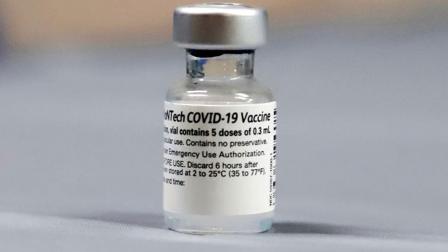
La Agencia Europea del Medicamento da su visto bueno a la vacuna de Pfizer
Compartir
Actualizada:
21 dic 2020 - 11:26
La Agencia Europea del Medicamento (EMA) dio este lunes su visto bueno a la vacuna desarrollada por Pfizer/BioNTech contra el coronavirus, el paso previo para que la Comisión Europea otorgue esta semana la licencia de uso condicional del fármaco en los países europeos.
La conclusión positiva fue alcanzada por los expertos de la EMA, que recibió de Pfizer el pasado 1 de diciembre la solicitud de comercialización de su vacuna en la Unión Europea (UE), aunque la agencia llevaba analizando en tiempo real los datos sobre la producción, dosificación y ensayos clínicos desde octubre, lo que le permitió llegar a estas conclusiones en tiempo récord.
La directora ejecutiva de la EMA, Emer Cooke, subrayó en rueda de prensa que la evaluación científica de sus expertos “se basa únicamente en la solidez de la evidencia científica sobre la seguridad, calidad y eficacia de la vacuna”.
Cooke aseguró que todos los estudios realizados, clínicos y no clínicos; “muestran de manera convincente que los beneficios son mayores que los riesgos” de aprobar esta vacuna para prevenir la covid-19.
Añadió que el comité de expertos en medicamentos humanos (CHMP) analizó miles de documentos “con datos adicionales que recibió incluso hasta este fin de semana”. Estos incluyen datos del ensayo de la vacuna en humanos, con la participación de unos 42.000 voluntarios. Ellos recibieron la vacuna o un placebo, para realizar esta “evaluación independiente” que concluyó este lunes con una recomendación positiva.
NUEVA CEPA
La directora de la EMA aseguró, por otra parte, que “no hay evidencias” de que la vacuna del covid-19 desarrollada por Pfizer/BioNTech no vaya a funcionar contra la nueva cepa de coronavirus detectada en Reino Unido.
Según Cooke, la última mutación que ha sufrido el SARS-CoV-2, dando lugar a una variante que se contagia con más rapidez, no ha sufrido suficientes cambios como para dejar sin eficacia a la vacuna de Pfizer, aunque insistió en que hay que hacer un seguimiento “cercano” a las campañas de vacunación hasta determinar el alcance de la inmunidad que provoca este fármaco.
TRANSPARENCIA
Cooke reconoció que la vacuna “solo ayudará a luchar contra la pandemia” si todos los ciudadanos europeos “tienen suficiente confianza en la autorización que será otorgada” al fármaco de Pfizer, por lo que prometió “transparencia a los ciudadanos para que puedan decidir sobre la vacunación en base a los hechos” y no a las teorías de la conspiración.
“La EMA publicará la información sobre la evaluación, incluidos todos los datos clínicos evaluados en la solicitud (de la autorización de comercialización condicional de Pfizer). Esto permitirá un mayor escrutinio independiente por parte de los científicos”, agregó.
Por su parte, Harald Enzmann, jefe del CHMP, recordó que “no hay evidencias de riesgos inaceptables” de la vacuna. Aunque destacó que hay “muy pocos datos sobre el uso de la vacuna en mujeres embarazadas porque no había suficientes casos de mujeres embarazadas en el ensayo clínico, así que se recomienda ir caso por caso, evaluando el riesgo individual en cada persona”.
VACUNA
Enzmann pidió “seguir usando mascarillas, lavarse las manos y mantener la distancia”; incluso después de recibir la vacuna, hasta que se pueda evaluar en una mayor población la eficacia de la inmunidad que provoca la vacuna.
Con esta evaluación de la EMA, la Comisión Europea puede ahora autorizar, previsiblemente el miércoles, el uso de la vacuna de Pfizer en los 27 países europeos, lo que permitirá a las autoridades sanitarias nacionales lanzar sus campañas de vacunación el 27 de diciembre, según espera Bruselas. EFE
Mire también
Compartir